Острые отравления 1,2-дихлорэтаном (ДХЭ) составляют одну из актуальных проблем современной клинической токсикологии, не смотря на то, что в последние годы количество интоксикаций, вызванных этим ядом, значительно снизилось. Причины не проходящего интереса к данной проблеме - значительная тяжесть и высокая летальность при наиболее часто встречающихся пероральных отравлениях ДХЭ. Минимальная смертельная доза яда для взрослого человека составляет 10 - 30 мл (Бандман А.Л. и др. 1990; Лужников Е.А. 1994), то - есть, равна примерно одному глотку. Видимо по этой причине среди интоксикаций ДХЭ преобладают тяжелые формы. По нашим данным, близким к литературным, на долю отравлений легкой, средней и тяжелой степени приходится 16, 10 и 74% соответственно. Нельзя признать удовлетворительными и результаты лечения. Так, по данным Е.А. Лужникова (1994) больничная летальность отравленных ДХЭ составляет около 50%. Еще выше этот показатель при тяжелых интоксикациях - как правило, 80 и выше процентов.
Отравления ДХЭ нередко развиваются на фоне алкогольного опьянения. По нашим данным подобная ситуация наблюдается примерно в 30 - 40% случаев. Общепринятая точка зрения состоит в том, что сочетание этанола с хлорированными углеводородами, в том числе и с ДХЭ, приводит к значительному повышению токсичности последнего (Беляков В.П., 1987; Демина В.И., Меркулов В.И., 1987). В то же время, клиническая практика отнюдь не всегда безоговорочно подтверждает эту позицию. Кроме того, в настоящее время считается (1,2-дихлорэтан. Гигиенические критерии 1990, Лужников Е.А. 1994), что токсичность ДХЭ, по крайней мере частично, определяется его биотрансформацией в 2-хлорэтанол (ХЭ), а ядовитость последнего - его метаболизмом в организме при участии тех же ферментных систем, которые определяют биотрансформацию этанола. Учитывая изложенное, представилось оправданным более детальное изучение влияния этанола на токсичность ДХЭ.
Материалы и методы исследования.
Материалы, положенные в основу этого сообщения, получены как путем клинического, так и экспериментального исследований. Клинические аспекты проблемы базируются на анализе 128 случаев острых пероральных отравлений ДХЭ тяжелой степени. Все обследованные - мужчины в возрасте от 18 до 60 лет, их средний возраст составляет 38,2 + 5,6 лет. В 52% отравления были случайными, в 38% - умышленными (с суицидной или демонстративной целью); в 10% причину установить не удалось. Из выборки исключены сочетания отравлений ДХЭ с другими экзогенными ядами (кроме этанола), механическими и термическими травмами, случаи интоксикаций ДХЭ у лиц с сахарным диабетом, наркоманией, хроническим алкоголизмом III степени, а так же длительным приемом некоторых лекарственных средств (психофармакологические препараты, циметидин и др.).
Диагноз отравления устанавливался на основании данных анамнеза, клиники заболевания, а также результатов химико-токсикологического исследования остатков яда и биосред пострадавших. Лечебные мероприятия на догоспитальном и госпитальном этапах включали реанимационные пособия по показаниям, удаление яда из желудочно-кишечного тракта, ранний гемодиализ или гемосорбцию, форсирование диуреза, инфузионную терапию с применением патогенетических и симптоматических средств (антиоксидантов, ингибиторов протеолиза, антиагрегантов, кровезаменителей, компонентов крови и т.д.)
При анализе клинических материалов все больные были разделены на три подгруппы: отравленные ДХЭ, у которых отравление произошло на фоне алкогольного опьянения или интоксикации (концентрация этанола в крови более 0,5 г/л), - I гр. (42); больные, у которых отравление ДХЭ возникло на фоне хронического алкоголизма I - II ст., однако не сочеталось с алкогольным опьянением или интоксикацией (концентрация этанола в крови менее 0,5 г/л) - II гр. (38). В третью группу вошли 48 больных, у которых отравления ДХЭ не сочеталось с алкогольным опьянением и (или) с хроническим алкоголизмом. Указанные группы не различались существенно по возрасту, срокам оказания и объему медицинской помощи. Всего в данном сообщении проанализированы 128 случаев тяжелых отравлений ДХЭ, соответствовавших указанным выше критериям.
Экспериментальная часть исследования выполнена на белых крысах-самцах массой 180 - 220 г. ДХЭ вводился однократно внутрижелудочно в масляном растворе. Животных подразделяли на группы: первая (контрольная) получала только ДХЭ [первоначально контроль имелся для каждой из групп опыта с введением, вместо этанола, аналогичного объема физиологического раствора. Однако отсутствие существенных различий в указанных группах по изучавшимся показателям позволило использовать для сравнение единые обобщенные данные ] ; животным второй группы в течение месяца до затравки вместо питьевой воды давали 20% раствор этанола (за 12 часов до введения ДХЭ раствор этанола заменили на воду); в третьей группе за 30 минут до ДХЭ однократно внутрь вводился этанол (3 мл/кг в виде 30% раствора); животным четвертой и пятой групп этанола (в 30% растворе) начинали вводить через 1 час после ДХЭ внутрибрюшинно - в первой из них в дозе 0,5 мл/кг, во второй - 2 мл/кг (первые три инъекции, далее по 1,5 мл/кг) через каждые 4 часа в течение первых суток после затравки ДХЭ; колебания концентрации этанола в крови животных, получавших 0,5 мл/кг, составляли в течение суток от 0,75 до 0,3 г/л, а во второй группе с разовой дозой спирта 2 мл/кг - от 3,2 до 1,8 г/л.
Оценивали показатели выживаемости, результаты наблюдения, а также концентрации яда и его метаболита ХЭ в крови животных. Определение концентрации ДХЭ, ХЭ и этанола осуществляли с помощью газовой хроматографии. Хроматография проводилась на приборах серии "Цвет". Определение этанола осуществлялось традиционным методом. Для идентификации и количественного анализа ДХЭ использовали ионизационно- пламенный детектор (ДИП); при определении ХЭ, наряду с ДИП, применяли также детектор электронного захвата. В качестве газа-носителя служил гелий. Скорость подачи водорода и гелия - 30, воздуха - 300 мл/мин. В качестве наполнителя колонок при анализе ДХЭ использовали Хроматон N-AW, 0,250 - 0,315 мм, пропитанный 15% Скваланом, Хроматон N-AW-DNCS, 0,160 - 0,200 мм, пропитанный 15% Реаплексом - 400, Хроматон N-AW, 0,200 - 0,250 мм, пропитанный Карбоваксом - 6000. Температура колонок 70 - 90oС, испарителя - 130oС. Для выделения ХЭ применяли Хроматон N-AW, 0, 200 - 0,250 мм, пропитанный 15% Полиэтиленгликолем. Температура колонки - 150oС, испарителя - 170oС.
Расчет показателей летальности (ЛД50) проводился с помощью пробит-анализа (Прозоровский В.Б. и др. 1978), результаты клинических наблюдений оценивали - по критерию X2, количественные результаты экспериментов - по T - критерию Стьюдента.
Результаты исследования.
При изучении материалов клинического обследования (Табл.1) данные, полученные у больных третьей группы (отравления, не связанные с алкогольным опьянением или хроническим алкоголизмом) рассматривались нами, как показатели своеобразного контрольного контингента. Анализ указанных материалов позволяет говорить о том, что большинство различий между выделенными нами группами проявляются в форме тенденций. Исключение составляют отдельные показатели, по которым различия являются статистически значимыми. Так, дозы яда, вызвавшие тяжелую интоксикацию у лиц с хроническим алкоголизмом достоверно ниже, чем в третьей группе наблюдения. Различие сохраняется, если исключить из анализа случаи с отравлениями сверхлетальными дозами ДХЭ - 100 и более мл. (36,3 + 4,1 мл и 51,5 + 6,4 мл, р < 0,05).
Таблица 1
Клиническая характеристика тяжелых отравлений 1,2-дихлорэтаном.
| Показатели | Группы наблюдения (абсолютные цифры/проценты) | Достоверность различий по группам | ||
| Группа I(n = 42) | Группа II(n = 38) | Группа III(n = 48) | ||
| Дозы яда (мл) | 69,5 +/- 12,2 | 50,4 +/- 5,0 | 74,0 +/- 8,2 | P2-3 < 0,05 |
| Энцефалопатия: | 42 (100) | 38 (100) | 48 (100) | |
| ? Легкая: | - | 7 (18,4) | 3 (6.2) | P1-2 < 0,05 |
| ? Умеренно выраженная: | 7 (14,7) | 14 (36,8) | 10 (21,0) | |
| ? Тяжелая: | 35 (85,3) | 17 (44,8) | 35 (72,8) | p1-2 < 0,05, p2-3 < 0,05 |
| Острая дыхательная недостаточность | 27 (64,3) | 16 (42,1) | 27 (56,2) | p1-2 < 0,05 |
| ? Центральная | 8 (19.0) | 2 (5,2) | 7 (14,6) | |
| ? Аспирационно-обтурационная | 9 (21,4) | 3 (7,9) | 7 (14,6) | p1-2 < 0,05 |
| ? Паренхиматозная | 4 (9,5) | 6 (15,8) | 5 (10,4) | |
| ? Смешанная | 8 (19,0) | 5 (13,2) | 8 (16,6) | |
| Острая сердечно-сосудистая недостаточность: | 36 (75,6) | 34 (89,4) | 43 (89,4) | |
| ? Первичный токсикогенный коллапс | 8 (19,0) | 3 (7,9) | 6 (12,5) | |
| ? Экзотоксический шок | 28 (66,6) | 31 (81,5) | 37 (76,9) | |
| Коагулопатия потребления (фаза гипокоагуляции) | 13 (30,9) | 16 (42,1) | 17 (35,3) | |
| Гастро-интестинальный синдром: | 42/100 | 38/100 | 48/100 | |
| ? Острый гастрит | 7 (16,7) | 7 (18,4) | 8 (16,6) | |
| ? Гастроэнтерит | 35 (83,4) | 31 (81,6) | 40 (83,4) | |
| Токсическая гепатопатия: | 36 (85,7) | 34 (89,4) | 40 (83,4) | |
| ? с умеренными ферментативными изменениями | 15 (35,7) | 5 (13,2) | 17 (35,6) | p1-2 < 0,05 p2-3 < 0,05 |
| ? со значительными изменениями | 21 (50,0) | 29 (76,2) | 23 (47,8) | p1-2 < 0,05 p2-3 < 0,05 |
| Летальность | 30 (71,2) | 34 (89,4) | 36 (74,8) | |
Что же касается клинических проявлений, то энцефалопатия в токсикогенной фазе регистрируется у всех пострадавших с тяжелыми отравлениями. При сочетании отравлений ДХЭ с алкогольным опьянением процент грубых расстройств сознания самый высокий, в то время как у лиц II группы более чем в половине случаев (55,2%) церебральные нарушения начального периода ограничиваются кратковременными фрагментарными расстройствами, атаксией, психомоторным возбуждением или умеренным угнетением, - то-есть проявлениями, более свойственными отравлениям ДХЭ средней тяжести, а в дальнейшем формируется типичная клиническая картина тяжелой интоксикации.
Более выраженные проявления энцефалопатии у лиц, отравленных ДХЭ на фоне алкогольного опьянения или интоксикации, находят отражение в структуре острой дыхательной недостаточности (ОДН). В этой группе преобладает ОДН центрального и аспирационно-обтурационного генеза (40,4%), в то время как у страдающих хроническим алкоголизмом подобные расстройства наблюдаются заметно реже (13,1%).
В I группе больных наиболее высок и процент пострадавших с первичным токсикогенным коллапсом. Это осложнение встречается, главным образом, в тех случаях, когда концентрация этанола в крови составляет около 2,5 - 3,0 г/л или более и отражает, судя по всему, известную способность этанола усиливать кардиоваскулярные нарушения при отравлениях хлорированными углеводородами. Что же касается экзотоксического шока, то наиболее часто он регистрируется у лиц, страдающих хроническим алкоголизмом. В этой же группе наиболее высок процент больных, у которых развивается выраженная коагулопатия потребления, хотя различия с другими группами не являются достоверными.
Гастро-интестинальные расстройства наблюдаются у всех пострадавших, а частота отдельных форм этих нарушений в группах практически не различается.
Некоторых предварительных уточнений требует оценка поражений печени. Поскольку смерть большинства отравленных ДХЭ тяжелой степени наступает в 1 - 2 сутки интоксикации, четкие клинические проявления гепатопатии успевают развиться далеко не всегда, а морфологические исследования практически у всех умерших через 8 - 12 часов после приема яда и позднее выявляют сходную картину дистрофии гепатоцитов и центрилобулярных некрозов. Для оценки выраженности гепатопатии мы использовали показатели сывороточной активности аминотрансфераз (АсАТ, АлАТ). К значительным нами отнесены увеличение этих показателей в 2 и более раза через 6 - 12 часов после приема яда, преобладающая активность АсАТ, а также элевация ферментативной активности в 5 и более раз к концу 1 суток. Энзимологические сдвиги обнаруживаются во всех группах наблюдения с примерно одинаковой частотой, однако у лиц, страдающих хроническим алкоголизмом, в 76% случаев эти изменения расценены нами, как значительные, тогда как в других группах данный показатель находится на уровне 48 - 50%.
Во второй группе наиболее высок и уровень больничной летальности. В других группах он примерно одинаков. Следует упомянуть о некоторых особенностях в динамике наступления летальных исходов. При тяжелых отравлениях ДХЭ наблюдается три пика указанных исходов - в первые 4 - 6 часов после приема яда, во второй половине первых - на вторые сутки и в конце первой недели интоксикации. Быстрое наступление смерти связано, главным образом, с глубокой комой, нарушениями дыхания, токсикогенным коллапсом и чаще наблюдается при сочетании отравления ДХЭ с алкогольной интоксикацией. Неблагоприятный исход в конце первых - начале вторых суток обусловлен преимущественно экзотоксическим шоком, чаще наблюдается у лиц, страдающим хроническим алкоголизмом, несколько реже - при "чистых" формах отравлений ДХЭ и еще реже - при сочетании ДХЭ с этанолом. Смерть в конце первой - начале второй недели наступала, в основном, от острой печеночной недостаточности, наблюдалась не часто (в пределах 10% от общего числа летальных исходов) и в отдельных группах наблюдения по частоте существенно не различалась.
Концентрации ДХЭ в крови отравленных на момент поступления в стационар колебалась в весьма широких пределах от 0,3 до 5,0 ммоль/л, в связи с чем средние показатели по группам больных достоверно не различались, хотя и наблюдалась тенденция к более низкому уровню яда у лиц, страдавших хроническим алкоголизмом. ХЭ в первые 2 - 3 часа после приема ДХЭ в биосредах отравленных либо не определялся, либо обнаруживался на уровне следов. Динамика показателей химико-токсикологического исследования крови в более поздние сроки была не характерна, главным образом в результате интенсивной элиминационной терапии, в том числе использования методов экстракорпоральной детоксикации. Сравнение данных химико-токсикологического исследования с клиническими проявлениями интоксикаций ДХЭ в ранние сроки позволяет считать, что наркотическая концентрация яда находятся на уровне 0,6 - 0,8 ммоль/л; у лиц, страдавших хроническим алкоголизмом, она достигает 1,0 ммоль/л, а при сочетании отравления с алкогольным опьянением снижается до 0,4 - 0,5 ммоль/л.
Таким образом, анализ клинических материалов позволяет считать, что наименее благоприятно протекают отравления ДХЭ на фоне хронического алкоголизма - при наиболее низких дозах яда у этой категории больных чаще, чем в других группах, формируется экзотоксический шок, более быстрыми темпами развиваются гепатоцеллюлярные поражения и наиболее высока больничная летальность. Иначе можно охарактеризовать больных, у которых отравление ДХЭ произошло на фоне алкогольного опьянения. Среди них наиболее высок процент выраженной начальной энцефалопатии, связанных с ней центральных, аспирационно-обтурационных и смешанных нарушений дыхания и первичного токсикогенного коллапса, но реже развивается экзотоксический шок и, как уже указано, процент летальности не выше, чем в группе, где отравления не сочетались с приемом алкоголя. Создается впечатление, что мнение об усилении ядовитости ДХЭ на фоне этанола главным образом связано с более выраженными церебральными расстройствами начального периода, дыхательными и кардиоваскулярными нарушениями, обусловленными неэлектролитными эффектами 1,2-дихлорэтана.
В то же время мы далеки от безаппеляционных оценок клинических материалов, главным образом потому, что некоторые критерии распределения больных по группам и отдельные клинические характеристики (оценка дозы, степени злоупотребления алкоголем, качество помощи на догоспитальном этапе) обладают относительной точностью.
Для того, чтобы оценить влияние этанола на токсичность ДХЭ в максимально стандартных условиях проведено экспериментальное исследование. Основанием для клинико-экспериментальных параллелей послужили данные литературы (1,2-дихлорэтан, Гигиенические критерии, 1990), а также собственные материалы, свидетельствующие о том, что в организме человека и животных (в частности крыс) метаболизм ДХЭ происходит сходным путями и темпами.
Результаты наблюдения за животными, отравленными ДХЭ (Табл. 2), позволяют говорить о том, что в группах, моделирующих клинические ситуации (I - контроль, II - длительно получавшие этанол до отравления, III - однократно получавшие этанол до введения ДХЭ) наблюдаются изменения, сходные с таковыми у больных аналогичных групп. Так, показатели ЛД50 наименьшие во II группе, а у животных I и III групп существенно не различаются. Длительность бокового положения (после введения ДХЭ в дозе 1,5ЛД50 контроля) наименьшая у крыс, предобработанных длительным введением этанола, а наибольшая (в I - III группах) у животных, однократно получавших этиловый спирт до ДХЭ. Во второй группе отмечено также наиболее быстрое наступление летальных исходов.
Представляют интерес и результаты экспериментов, в которых этанол вводился после затравки ДХЭ в малых (IV группа) и больших (V группа) дозах. Показатели четвертой группы достоверно не отличались от контроля. У животных пятой группы выявлены наиболее существенные различия с контрольными - самые высокие значения ЛД50. наибольшая длительность бокового положения и позднее развитие летальных исходов (после введения ДХЭ в дозе 1,5ЛД50 контроля).
Таблица 2
Некоторые показатели токсичности ДХЭ на фоне различных режимов введения этанола.
| Группы животных | Показатели | ||
| ЛД50 ДХЭ (мг/кг) | Длительность бокового положения (мин) | Сроки гибели в 1 - 2 сутки (часы) | |
| I | 712.0 +/- 32,4 | 220,0 +/- 18,6 | 16,8 +/- 2,0 |
| II | 526,4 +/- 42,1** | 137.0 +/- 20,4 | 10,2 +/- 1,6* |
| III | 690,3 +/- 43,5 | 292,0 +/- 15,4 | 18,9 +/- 2,4 |
| IV | 736,3 +/- 34,8 | 263,0 +/- 30,1 | 19,6 +/- 1,8 |
| V | 1132,0 +/- 52,3** | 646,0 +/- 52,5** | 28,6 +/- 3,4** |
Определение концентрации ДХЭ в крови также выявляет наиболее выраженные различия у животных II и V групп (Табл.3), причем показатели II группы ниже, а V - достоверно выше, чем в контроле. Кроме того, в группе III отмечается тенденция к более высокому уровню ДХЭ, особенно через 3 часа после затравки, однако различие с показателями контроля не достоверны.
Несколько иначе выглядят результаты определения хлорэтанола (Табл.4) - в V группе они значительно выше контрольных, в III и IV - только соответственно через 3 и 12 часов после затравки; в крови животных II группы концентрация хлорэтанола (ХЭ) во всех точках определения несколько ниже контроля, однако различие статистически не достоверно.
Таблица 3
Концентрация ДХЭ (мМ/л) в крови крыс, отравленных дихлорэтаном
| Группы животных | Время после затравки (часы) | ||
| 3(n = 7) | 6(n = 7) | 12(n = 7) | |
| I | 0,728 +/- 0,050 | 0,326 +/- 0,031 | 0,121 +/- 0,020 |
| II | 0,472 +/- 0,054** | 0,123 +/- 0,025* | 0,062 +/- 0,004** |
| III | 0,846 +/- 0,069 | 0,354 +/- 0,040 | 0,134 +/- 0,028 |
| IV | 0,738 +/- 0,072 | 0,298 +/- 0,042 | 0,092 +/- 0,007 |
| V | 0,920 +/- 0,052** | 0,449 +/- 0,038** | 0,212 +/- 0,032** |
Концентрация ХЭ (mМ/л) в крови крыс, отравленных дихлорэтаном
| Группы животных | Время после затравки (часы) | ||
| 3(n = 7) | 6(n = 7) | 12(n = 7) | |
| I | 2,92 +/- 0,61 | 4,18 +/- 0,76 | 3,02 +/- 0,56 |
| II | 2,06 +/- 0,35 | 3,12 +/- 0,37 | 2,18 +/- 0,30 |
| III | 4,47 +/- 0,42** | 3,97 +/- 0,58 | 3,44 +/- 0,46 |
| IV | 3,21 +/- 0,46 | 4,68 +/- 0,52 | 4,68 +/- 0,52* |
| V | 6,88 +/- 0,90** | 8,97 +/- 0,65** | 7,21 +/- 0,74** |
* - р < 0,05: ** - р < 0,01 -0.001
Таким образом, суммируя результаты экспериментов, можно обобщить полученные данные следующим образом: животные, получавшие этанол однократно перед затравкой ДХЭ или в течение суток в малых дозах после нее по большинству изучавшихся показателей существенно не отличаются от контрольных. Длительная предобработка животных этанолом приводит к значительному усилению токсического действия ДХЭ и более быстрому падению концентрации неизмененного яда в крови. Введение высоких доз этанола после ДХЭ сопровождается снижением летального действия последнего на фоне заметного усиления наркотических эффектов, увеличения концентрации неизмененного дихлорэтана в крови и, особенно, его метаболита - хлорэтанола.
Обсуждение результатов
Сравнивая полученные нами клинические данные с материалами других авторов, изучавших этот вопрос, мы можем отменить их совпадение в ряде частностей при некотором различии в общей оценке. Так, по мнению В.П. Белякова (1987), сочетание отравлений ДХЭ с употреблением этанола приводит к увеличению процента летальных исходов в первые 4 часа интоксикации при явлениях агонии и комы, в то время как при "чистом" отравлении ДХЭ основной причиной смерти является острая сердечно-сосудистая недостаточность. По нашим данным сочетание ДХЭ с этанолом вызывает увеличение глубины комы, церебральных и аспирационно-обтурационных нарушений дыхания и сопровождается тенденцией к нарастанию частоты токсикогенного коллапса в ранние сроки интоксикации, однако реже приводит к формированию экзотоксического шока. Цитированный выше автор приходит к выводу о существенном увеличении токсичности ДХЭ при сочетании его с этанолом. По нашему мнению этанол усиливает те ранние проявления интоксикации ДХЭ, которые обусловлены наркотическими эффектами яда, однако это не влечет за собой существенных изменений интегрального показателя его токсичности - больничной летальности.
Интерпретацию результатов клинического и экспериментального исследования целесообразно проводить на основе существующих представлений о механизмах действия ДХЭ. В настоящее время считается, что токсичность ДХЭ обусловлена как неизмененной молекулой яда, так и продуктами его метаболизма в организме. С действием собственно ДХЭ связаны, главным образом, церебральные нарушения раннего периода, обусловленные наркотическим свойствами яда, кардиодепрессия, гемолиз и т.д. Однако главная роль в реализации токсичности ДХЭ отводится его метаболитам (Рис.1).
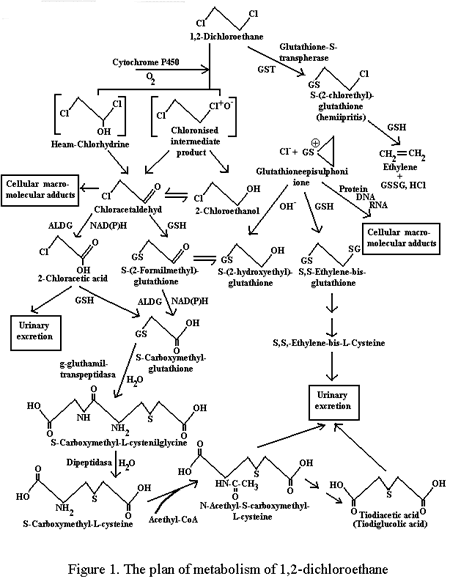
Начальной фазой метаболизма ДХЭ является его расщепление при участии двух ферментативных систем: неспецифической монооксигеназной системой микросом (НМСМ), ассоциированной с цитохромом Р450 и цитозольной глутатион-S-трансферазой (Г-S-Т), причем основная роль отводится НМСМ. Взаимодействие ДХЭ с Г-S-Т приводит к образованию полуиприта и иона глутатионэписульфония, обладающего алкилирующими свойствами. Этот путь метаболизма определяет, главным образом, повреждения ДНК и, судя по всему, не играет важной роли в реализации острой токсичности яда.
Под влиянием НМСМ, основной системы метаболизма ДХЭ. возможно образование гемхлоргидрина и хлорозированного промежуточного продукта, который обозначается также как реактивный галозокомплекс. Эти соединения, по всей вероятности не ферментативным путем, трансформируются в 2-хлорацетальдегид (ХАА) и 2-хлорэтанол, которые, в свою очередь, под влиянием алкоголь- (АДГ) и альдегиддегидрогеназы (АльДГ) превращаются в монохлоуксусную кислоту (МХУК). ХАА и МХУК соединяясь с восстановленным глутатионом, дехлорируются, превращаясь в продукты с низкой биологической активностью. На одном из этапов этих превращений дехлорированный дериват ХАА, соединенный с глутатионом, метаболизируется АльДГ.
Представленная схема метаболизма ДХЭ в организме является в настоящее время наиболее признанной. Вместе с тем мнения различных авторов о том, какие из образовавшихся продуктов биотрансформации ДХЭ определяют его токсичность, совпадают не всегда. Так, по мнению И.Г. Мизюковой, М.Г. Кокаровцевой (1978) подобным метаболитом является ХАА и МХУК, в то время как Т.В. Новиковская, Ж.А. Лисовик (1988) считают ведущим процессом активацию ПОЛ, которая может быть инициирована промежуточными продуктами метаболизма ДХЭ, такими, например, как реактивный галозокомплекс.
Рассматривая указанные выше процессы с позиций возможного влияния на них различных режимов поступления в организм этанола, можно выделить несколько участков метаболической цепочки, где это влияние наиболее вероятно, и, в то же время, разнонаправлено при длительном предварительном употреблении этанола и его присутствии в биосредах на фоне интоксикации ДХЭ. Речь идет, прежде всего, о первой фазе метаболизма, осуществляемого НМСМ. Длительная предобработка этанолом вызывает индукцию НМСН, о чем свидетельствует достоверное уменьшение длительности гексеналового сна (в наших опытах - с 32,8 + 2,6 в контроле до 20,6 + 1,8 мин в опыте; р < 0,01). Влияние этой индукции на метаболизм ДХЭ подтверждается наиболее низкими концентрациями яда в крови животных данной группы, а также увеличением их летальности.
Нельзя полностью также исключить роль индукции микросомальной этанол окисляющей системы (МЭОС), которая, как известно (Лакин К.М., Крылов Ю.Ф., 1981) наблюдается при длительном введении этанола. Эта индукция может иметь значение для биотрансформации ХЭ, о чем косвенно свидетельствует отсутствие существенного повышения концентрации данного метаболита в крови животных, прошедших длительную предобработку этиловым спиртом, на фоне интенсификации у них начальной стадии метаболизма ДХЭ. Однако указанная возможность нуждается в дальнейшем изучении, поскольку участие МЭОС в биотрансформации ХЭ точно не установлено.
Иная ситуация складывается когда ДХЭ и этанол одновременно присутствуют в биосредах. В подобных условиях этанол, действуя целой молекулой, способен усиливать неэлектролитные эффекты ДХЭ, что проявляется увеличением глубины и продолжительности коматозных состояний, а также тенденцией к повышению частоты связанных с комой расстройств дыхания и гемодинамики в ранние сроки интоксикации. Влияние этанола на метаболизм ДХЭ может осуществляться двумя основными механизмами - за счет самого спирта и его метаболитов, в первую очередь ацетальдегида. Первый может реализоваться, главным образом, на двух стадиях биотрансформации - микросомальной и превращения ХЭ в МХУК.
Возможность торможения этанолом микросомального метаболизма ДХЭ подтверждается увеличением концентрации дихлорэтана в крови животных, получавших высокие дозы спирта, причем не только в первые часы, когда этот эффект может быть связан с увеличением всасывания яда, но и через 12 часов после затравки. Механизм подавления этанолом биотрансформации ДХЭ не ясен и требует дополнительного изучения.
Весьма значимой представляется другая возможность влияния этанола на метаболизм ДХЭ - путем торможения превращения ХЭ в ХАА и далее в МХУК. Способность этилового спирта конкурировать с ХЭ за АДГ не вызывает сомнений и подтверждается как данными литературы (Бонитенко Ю.Ю. и др. 1981, Johnson M.K., 1967, Peterson D.I. et al, 1968), так и ранее полученными нами материалами по изучению метаболизма ХЭ, в гомогенатах печени - подавление скорости битрансформации ХЭ было тем выраженнее, чем выше использованные концентрации этанола. Способность этилового спирта тормозить метаболизм ХЭ подтверждают и результаты настоящего исследования - у животных V группы, отравленных ДХЭ, концентрация ХЭ в крови на фоне введения высоких доз этанола была значительно выше, чем в контроле. Указанный эффект в III и IV группах зарегистрирован лишь частично (соответственно в ранние и более поздние сроки с момента введения ДХЭ), по-видимому потому, что в первой из них этиловый спирт применялся однократно, а во второй - в малых дозах, не способных действенно конкурировать с ХЭ за АДГ.
Сложнее оценить влияние ацетальдегида, образующегося в процессе метаболизма этанола, на биотрансформацию ДХЭ. Наиболее вероятно это влияние может реализоваться на стадии трансформации ХАА в МХУК путем конкуренции двух альдегидов за АльДГ. Данные, представленные в настоящем сообщении, не позволяют оценить указанную возможность. В то же время ее изучение представляется важным. Косвенно об этом свидетельствуют полученные нами результаты влияния цианамида кальция (ингибитора АльДГ) в сочетании с амидом изовалериановой кислоты (ингибитором АДГ) на токсичность ДХЭ (Bonitenko U.U., et al. 1998) - применение подобного сочетания приводит в эксперименте к существенному увеличению показателя ЛД50 дихлорэтана.
Конечно, было бы большим упрощением сводить влияние различных режимов введения этанола на токсичность ДХЭ лишь к эффектам, связанным с обсужденными выше возможностями модификации токсикокинетики яда и его метаболитов и не учитывать многочисленные и разнообразные биохимические и функциональные изменения, вызываемые этиловым спиртом. Хорошо известно, что острое и хроническое применение этанола стимулирует перекисное окисление липидов, вызывает перераспределение окисленных и восстановленных форм коферментов, влияет на ферменты метаболизма глутатиона, содержание его -SH и S-S форм и т.д. (Новиков Н.Г., 1985; Sippel H.W., 1983; Yuki T. Et al., 1989). Однако, полученные нами данные и материалы, изложенные в литературе (Guengerich F.P. et al, 1980, Шилов В.В., 1997, 1999), позволяют говорить о том, что наряду с неэлектролитными эффектами, во влиянии этанола на токсичность ДХЭ заметное место занимает модификация микросомального метаболизма и воздействие этилового спирта на превращение хлорэтанола в монохлоруксусную кислоту, причем последнее в существенной мере определяет специфичность действия яда.
Список литературы
1. Бандман А.Л., Войтенко Г.А., Волкова Н.В. и др. Вредные химические вещества. Углеводороды. Галогенпроизводные углеводородов. - Л.: Химия, 1990 - 732 с.
2. Беляков В.П.О влиянии этанола на течение отравлений дихлорэтаном. // 2-ой Всеросс. Съезд суд. медиков. Иркутск. 1987. - с 224 - 225
3. Бонитенко Ю.Ю., Бочаров Н.В., Лишенко В.В. Влияние этилового спирта на некоторые показатели токсичности этиленхлоргидрина. //Гигиена труда и проф. заболевания. - 1981, ?9. - с. 44 - 45
4. Bonitenko U.U., Bonitenko E.U., Poisoning with alcohols - some clinical and experimental aspects. Arch Toxicol Kinet Xenobiot Metab 1998; 6(3): 341-6
5. 1,2 - Dichlorethan. Health and Safety guide 1990; 62: 1-80
6. Демина В.И., Меркулова В.И. К судебно-медицинской экспертизе сочетанных отравлений алкоголем. // 2-ой Всеросс.Съезд суд. медиков. Иркутск. 1987. - с 219 - 220
7. Guengerich F.P., Crawford W.V., Domaradzki J.Y., Macdonald T.L., Watanabe P.G. In vitro activation of 2-dichlorethane by microsomal and cytosolic enzymes. Toxicol Appl Pharmacol 1980; 55: 303-17
8. Johnson M.K. Metabolism of chloroethanol in the rats. Biochem Pharmacol 1967; 16(1): 185
9. Лакин К.М., Крылов Ф.Ю. Биотрансформация лекарственных средств. М.: Медицина. 1981 - 344 с.
10. Лужников Е.А. Клиническая токсикология. - М.: Медицина. 1994. - 256 с.
11. Мизюкова И.Г., Кокаровцева М.Г. Лечебная эффективность ацетилцистеина при остром отравлении дихлорэтаном. // Фармакол. Токсикол. - 1978. - 41,?3. - с. 350 - 354
12. Новиковская Т.В., Лисовик Ж.А. Применение специфической терапии при острых отравлениях дихлорэтаном. // Сб. науч. Трудов. Мос.гор. НИИ скорой помощи. - 1988. - 74. С. 106 - 112
13. Новиков Н.Г. Нарушение окислительных процессов в сердце и печени при интоксикации этанолом и коррекция их глютаматом и сукцинатом. Автореф. дис. : канд. биол. наук. Челябинск. - 1985. - 25 с.
14. Peterson D.I., Peterson J.E., Hardinge V.G. Protection by ethanol against the toxic effects of vonofluoroethanol and monochloroethanol. J Pharmacy Pharmacol 1968; 20(6): 465-8
15. Прозоровский В.Б., Прозоровская М.П., Демуенко В.М. Экспресс-метод определения средней эффективной дозы и ее ошибки // Фармакол и Токсикол - 1978. - Т. 41,?4. - с. 497 - 502
16. Шилов В.В., Плужников Н.Н., Софронов Г.А. Модификация токсикокинетики и токсикодинамики дихлорэтана с использованием перфторана // Перфторуглеродные соединения в биологии и медицине. - 1997, ?8. - с. 46 - 52
17. Шилов В.В. Детоксикационная терапия острых отравлений липофильными ксенобиотиками с помощью перфторуглеродных соединений. Автореф. дис. : доктора мед. наук. С-Петербург. - 1999. - 43с.
18. Sippel H.W. Effect of an acute dose of ethanol on lipid peroxidation and on the activity of microsomal glutathion-S-transferase. Acta Pharmacol Toxicol 1983; 53(2): 135-40
19. Yuki T., Yoshitoku K., Nakagava Y., Ohashi K. et. al. Changes in hepatic lipid peroxidation after acute and chronic ethanol treatment || Med Biochem Chem Aspects Free Radicals. Kyoto. - 1989. Vol.2. Amsterdam - 1989. P. 967-70



 Федеральное государственное бюджетное учреждение науки
Федеральное государственное бюджетное учреждение науки
