Санкт-Петербург, 2002 г.
РАЗДЕЛ 7. ИЗБИРАТЕЛЬНАЯ ТОКСИЧНОСТЬ
ГЛАВА 7.4.
Гематотоксичность
Гематотоксичность это свойство химических веществ, действуя на организм немеханическим путём, избирательно нарушать функции клеток крови или её клеточный состав (как в сторону уменьшения, так и увеличения числа форменных элементов). Важнейшими функциями клеток крови являются: кислородтранспортная, гемостатическая, обеспечение иммунитета. Нарушение числа форменных элементов может явиться следствием прямого разрушения клеток в кровяном русле, повреждения процессов клеточного деления и созревания в кроветворных органах, поступления зрелых элементов в кровь.
Частыми проявлениями гематотоксичности являются: нарушение свойств гемоглобина (метгемоглобинемия, карбоксигемоглобинемия), анемии (в том числе гемолитические), тромбоцитопении, лейкопении, лейкемии. По большей части клеточные дискразии, вызванные токсикантами, обратимы и исчезают после прекращения действия вещества. Однако встречаются и персистирующие формы, заканчивающиеся летальным исходом в случае тяжелого повреждения костного мозга.
1. Гемопоез
Гемопоэзом называется процесс амплификации и дифференциации клеточных элементов крови, в ходе которого ограниченное количество стволовых клеток даёт начало более дифференцированным делящимся клеткам, которые, в свою очередь, превращаются в созревающие, а затем и зрелые форменные элементы. "Родоначальницей" клеток является полипотентная стволовая клетка (ПСК), при делении которой образуются клетки - предшественницы всех клеточных элементов. По завершении эмбриогенеза ПСК остается единственным элементом, отвечающим за репродукция клеток крови. В норме у взрослого человека гемопоэз осуществляется в костном мозге, который представлен кластерами гемопоэтических клеток рассеянных в эпифизах трубчатых костей, плоских костях черепа, грудине, позвонках, костях таза, рёбрах. Даже в условия экстремального гемопоэтического стресса, развивающегося например при трансплантации костного мозга, экстрамедуллярное кроветворение в печени, селезёнке, лимфатических узлах у взрослого отмечается крайне редко. Пул гемопоэтических клеток-предшественников и пул зрелых форменных элементов крови находятся в состоянии динамического равновесия, при котором гибель и разрушение зрелых клеток уравновешено постоянной продукцией и выходом в кровь молодых. В среднем, у взрослого человека в сутки разрушается и заново образуется от 200 до 400 млн. клеток крови. Повреждающее действие на процесс гемопоэза сопровождается не только гибелью, нарушением дифференциации и созревания клеток, но и активацией значительной части стволовых клеток, в нормальных условиях находящихся в состоянии покоя.
2. Нарушение функций гемоглобина
Одна из важнейших функций крови - транспорт кислорода от легких к тканям. Транспорт кислорода осуществляется двумя способами:
- в форме соединения - гемоглобином;
- в форме раствора - плазмой.
В растворенном состоянии плазмой крови переносится около 0,2 мл О2 на 100 мл крови. В связанной с гемоглобином форме эритроциты переносят в 100 раз больше кислорода (20 мл на 100 мл крови). 1 г гемоглобина способен обратимо связать около 1,5 мл О2, а в 100 мл крови содержится около 14 - 16 г гемоглобина.
В результате взаимодействия кислорода с гемоглобином образуется нестойкое соединение оксигемоглобин (HbО) (рисунок 1).
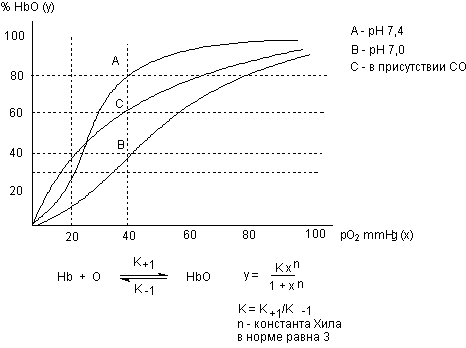
Рисунок 1. Кривая насыщения гемоглобина кислородом
При повышении парциального давления кислорода в среде (сатурация крови в легких) содержание НbО увеличивается и при 100 mmHg приближается к 100%. При понижении парциального давления О2 (в тканях) НbО распадается, при этом кислород выделяется в среду и утилизируется тканями организма. Процесс насыщения и рассыщения гемоглобина О2 описывается S-образной кривой. Такая форма зависимости между рО2 и %НbО есть следствие явления взаимодействия субъединиц гемоглобина в молекулярном комплексе (гем-гем взаимодействие), физиологический смысл которого - обеспечение максимально возможного выделения кислорода в ткани при незначительном различии парциального давления газа в крови и тканях (рО2 крови - около 40 mmHg; рО2 тканей - около 20 mmHg; выделяется около 50% связанного кислорода).
В норме на сродство кислорода к гемоглобину влияют многочисленные факторы. Среди основных: рН, рСО2 (эффект Бора), биорегуляторы процесса диссоциации оксигемоглобина (2,3-дифосфоглицерат).
Из сказанного ясно, что вещества, взаимодействующие с гемоглобином и изменяющие его свойства, будут существенно нарушать кислородтранспортные свойства крови, вызывая развитие гипоксии гемического типа.
2.1. Метгемоглобинообразование
В процессе жизнедеятельности железо гемоглобина постоянно окисляется, превращаясь из двухвалентной в трёхвалентную форму. Гемоглобин, железо которого трёхвалентно, называется метгемоглобином. Метгемоглобин не участвует в транспорте кислорода, поэтому в нормальных эритроцитах постоянно идёт процесс восстановления образующегося метгемоглобина в гемоглобин. Эритроциты, содержащие метгемоглобин, склонны к гемолизу. Физиологический уровень метгемоглобина в крови - менее 1%. Высокое содержание метгемоглобина, развивающееся как правило в результате действия некоторых токсикантов, приводит к нарушению кислородтранспортной функции крови, а спустя некоторое время и гемолизу, что сопровождается снижением парциального давления кислорода в тканях, развитию тяжёлой гипоксии.
Поддержание метгемоглобина на уровне менее 1% обеспечивается двумя физиологическими механизмами.
Первый связан с восстановлением или связыванием ксенобиотиков-окислителей до момента их действия на гемоглобин. Так, в присутствии энзима глутатионпероксидазы (ГПО) восстановленный глутатион взаимодействует с молекулами-окислителями, попавшими в эритроциты, предотвращая их метгемоглобинобразующее действие. Недостаток субстратов, поддерживающих содержание оксидантов в эритроцитах на низком уровне, может привести к накоплению этих веществ, умеренной метгемоглобинемии, гемолизу и появлению в крови телец Гейнца. Тельца Гейнца представляют собой продукты денатурации гемоглобина. Механизм, посредством которого окислители вызывают их образование и взаимоотношения этого процесса с метгемоглобинообразованием остаются не выясненными.
Второй механизм обеспечивает восстановление образовавшегося в крови метгемоглобина до гемоглобина при участии двух ферментативных систем (рисунок 2).
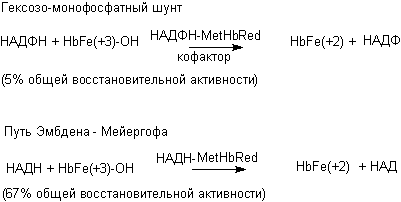
Рисунок 2 Механизмы восстановления метгемоглобина
В обеих системах донорами электронов (редуцирующие агенты) являются продукты анаэробного этапа метаболизма глюкозы и гексозомонофосфатного превращения. Поскольку в эритроцитах отсутствуют энзимы цикла трикарбоновых кислот и цепь дыхательных ферментов, единственными источниками энергии в клетках являются как раз гликолиз и гексозомонофосфатный шунт. В количественном отношении более значимыми являются механизмы связанные с гликолизом (95% восстановительной активности in vivo; 67% общей восстановительной активности in vitro). Основным донором электронов для процесса восстановления метгемоглобина является восстановленный никатинамидадениндинуклеотид (НАДН). Система достигает полного развития к 4 месяцу жизни новорожденного.
В процессе гексозомонофосфатного превращения под влиянием гексозо-6-фосфатдегидрогеназы (Г-6ф-ДГ) образуется восстановленный никатинамидадениндинуклеотд фосфат (НАДФН), который не только участвует в превращении метгемоглобина в гемоглобин в присутствии НАДФН-метгемоглобинредуктазы, но и переводит окисленный глутатион в восстановленную форму (последний связывает ксенобиотики-окислители - см. выше). Поэтому недостаток НАДФН также может сопровождаться образованием телец Гейнца.
2.1.1. Причины метгемоглобинообразования
Метгемоглобинемией называется состояние, при котором в крови определяется более 1% метгемоглобина. Метгемоглобинемия бывает врождённой и приобретённой. Приобретенная метгемоглобинемия развивается в результате действия на организм некоторых лекарств, промышленных и экотоксикантов, которые либо непосредственно окисляют железо, входящее в структуру гемоглобина, либо метаболизируют в организме с образованием реактивных продуктов, обладающих этим свойством (таблица 1).
Таблица 1. Перечень основных метгемоглобинобразователей
аллоксон альфа нафтиламин аминофенол (и его производные) аммония нитрат анилин (и его производные) антипирин арсин ацетанилид бензол (и его производные, в том числе нитропроизводные) бензокаин диаминодифенилсульфон диметиламин динитрофенол динитротолуол гидразин гидрохинон гидроксиламин лидокаин матиленовый синий нафтиламин нитриты (в том числе органические) нитраты (в том числе органические) нитропрусид натрия оксиды азота |
нитрофураны нитроглицериннитрофенол озон пара-аминопропиофенол пара-толуидин перекись водорода плазмохин пиридин пирогаллол пиридин сульфанол сульфонамиды дапсон пронтозил сульфаниламиды сульфатиазол сульфоны тетралин толулдиамнтолуидин тринитротолуол трионал и т.д.фенацетин фенолы фенилендиамин фенилгидразин хлораты хлоранилин хлорбензол хлорнитробензол |
Скорость образования метгемоглобина у различных экспериментальных животных при введении им веществ, подвергающихся в организме активации, как правило существенно различается (таблица 2).
Таблица 2. Способность некоторых ароматических аминов вызывать метгемоглобинэмию у разных экспериментальных животных
Вещества |
Максимальный уровень МеtHb в крови (%) |
|
Кролик |
Собака |
|
Анилин |
5 |
63 |
2-аминофлюорен |
6 |
45 |
4-аминобифенил |
40 |
85 |
р-аминофенол |
1 |
60 |
Фенилгидроксиламин |
47 |
40 |
Врождённая метгемоглобинемия является следствием дефекта структуры молекулы гемоглобина (М-гемоглобин), либо недостаточности ряда редуктаз.
2.1.1.1. Врожденная метгемоглобинемия
Врожденная метгемоглобинемия может быть обусловлена синтезом в организме гемоглобина М. Гемоглобин М представляет собой изменённую молекулу гемоглобина, с необычным аминокислотным составом
Наиболее частой причиной врождённых метгемоглобинемий является дефицит НАДН - метгемоглобинредуктазы. Лица с дефектом этого энзима справляются с перманентным образованием метгемоглобина в нормальных условиях за счет эритроцитарной НАДФН - метгемоглобинредуктазы и редуцирующих субстратов. Эта патология также генетически обусловлена и передаётся как по гетерозиготному, так и по гомозиготному механизму.
Уровень метгемоглобина в крови у пациентов с гомозиготной недостаточностью составляет 10 - 50%. Клинически патология проявляется цианозом. Кроме того у больных с содержанием метгемоглобина 40% и более отмечается диспное, быстрая утомляемость, частая головная боль. Ежедневный прием метиленового синего или больших доз аскорбиновой кислоты позволяет поддерживать метгемоглобинемию на уровне 10%. У больных с гетерозиготной недостаточностью НАДН - редуктазы уровень метгемоглобина в крови - до 2%, однако они чрезвычайно чувствительны к действию метгемоглобинобразующих токсикантов.
Врождённый дефицит НАДфН - редуктазы встречается редко. Поскольку энзим имеет небольшое функциональное значение, в крови отмечается нормальное содержание гемоглобина.
При врождённом дефиците Г-6Ф-ДГ отмечается пониженное содержание НАДФН и глутатиона в эритроцитах. В этих условиях повышается содержание оксидантов в клетках, вызывающих образование метгемолглобина, гемолиз, анемию, появление в крови телец Гейнца. У таких лиц особенно тяжело протекают инфекционный или токсический процессы. Нередко развивается острый гемолитический криз, особенно при действии токсикантов со свойствами оксиданта. В этих ситуациях назначение восстановителей не предотвращает бурное развитие метгемоглобинообразования.
2.1.1.2. Приобретённая метгемоглобинемия
Метгемоглобинемия развивается в тех случаях, когда скорость образования метгемоглобина под влиянием токсикантов превышает скорость его обратного превращения в гемоглобин. В этой связи тяжесть патологии определяется скоростью поступления ксенобиотика в организм, а затем в эритроциты, его окислительным потенциалом, дозой, скоростью элиминации. Если действующим агентом является не исходное вещество, а продукт его метаболизма, то глубина патологического процесса зависти также от интенсивности процесса биоактивации. Химизм реакции метгемоглобинообразования для большинства токсикантов не установлен.
2.1.2. Краткая характеристика некоторых токсикантов
2.1.2.1. Анилин
Анилин - вязкая, бесцветная жидкость, темнеющая на свету и воздухе. Применяется в производстве лекарственных веществ, антиоксидантов, фотоматериалов, красителей и др.
Действуя ингаляционно, через кожу и желудочно-кишечный тракт анилин может вызывать тяжелую патологию. По мимо метгемоглобинемии развивается гемолитическая анемия с образованием телец Гейнца.
Механизм действия анилина до конца не установлен. Известно, что in vitro, при инкубации с суспензией эритроцитов, вещество не вызывает метгемоглобинообразования. Вместе с тем, метаболиты анилина: фенилгидроксиламин, 2-аминофенол, 4-аминофенол - вызывают образование метгемоглобина in vitro. Полагают, что с учетом скорости накопления каждого из упомянутых метаболитов в организме и их индивидуальной активности, относительное значение фенилгидроксиламина, 2-аминофенола и 4-аминофенола в образовании метгемоглобина при отравлении анилином может быть оценено соответственно, как 100:4:1 (рисунок 3).
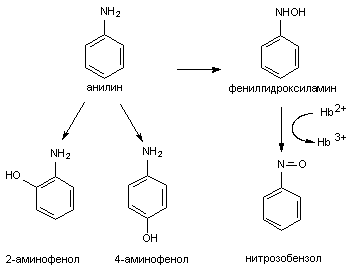
Рисунок 3. Схема метаболизма анилина
Поскольку анемия развивается спустя несколько суток после острой интоксикации анилином, по завершения лечебных мероприятий по поводу метгемоглобинемии, отравленные анилином должны находиться под наблюдением врача в течение относительно длительного времени.
2.1.2.2. Дапсон (4,4-диаминодифенилсульфон)
Дапсон - синтетический сульфон, структурно напоминающий сулфаниламиды (рисунок 4).
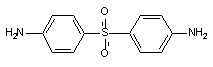
Рисунок 4. Структура дапсона
Препарат используют для лечения лепры, герпетиформных дерматитов, профилактики малярии (комбинированный препарат Маолирим), гангренозных пиодермитов, пустулёзного псориаза, плоского лишая и т.д. В последние годы препарат, совместно с сульфаметаксозолом, применяют для лечения воспаления лёгких, вызванного Pneumocystis carinii, у больных СПИД.
Токсичность дапсона связана с формированием в ходе его метаболизма гидроксиламин-производных, являющихся метгемоглобинобразователями (см. выше). Терапевтический индекс препарата низок и дозы более 200 мг/кг при продолжительном приёме могут стать причиной анемизации с образованием характерных телец Гейнца. С целью недопущения образования метгемоглобина в крови больных иногда прибегают к длительному введению метиленового синего. В результате передозировки дапсона может развиться и сульфметгемоглобинемия. Сульфгемоглобин - продукт необратимого окисления гемоглобина некоторыми токсикантами. Гемолиз, как правило, развивается спустя 6 - 9 дней после действия токсиканта. Максимум летальных исходов отмечается на 4 - 6 сутки. Снизить выраженность интоксикации удаётся путём промывания желудка, назначением больших доз активированного угля. Эффективность гемоперфузии, гемодиализа, форсированного диуреза не доказана.
2.1.2.3. Нитриты
Эффект могут вызывать как органические, так и неорганические вещества, содержащие в молекуле нитрогруппы. Неорганические нитриты это соли азотистой кислоты (азотистокислый натрий - NaNO2). Кристаллические вещества, хорошо растворимые в воде. Они применяются в производстве органических красителей. Органические нитриты представляют собой эфиры азотистой кислоты (амилнитрит, пропилнитрит и т.д.), содержащие в молекуле одну или несколько нитритных групп (-О-N=О), связанных с органическим радикалом. Это бесцветные или бледно-желтые летучие жидкости, плохо растворимые в воде. Используются в органическом синтезе и как сосудорасширяющие и спазмолитические средства (нитроглицерин и др.). Нитриты - типичные метгемоглобинообразователи.
Приём нитроглицерина может приводить к образованию метгемоглобина. Обычная доза препарата (4,8 мг. под язык) не вызывает клинически значимого эффекта (до 0,5%). Патологическое состояние может сформироваться при приёме очень большой дозы вещества лицами с анемией, почечной или печеночной недостаточностью.
Встречаются токсикомании, обусловленные пристрастием к ингаляции амилнитрита, бутилнитрита и других летучих нитросоединений. По свидетельству токсикоманов эти вещества вызывают длительно продолжающееся ощущение оргазма. В таких случаях имеется реальная угроза смертельной интоксикации метгемоглобинобразователями. У лиц с врожденной недостаточностью эритроцитов, например дефицитом Г-6Ф-ДГ, ингаляция веществ может привести к массивному гемолизу.
Определённую опасность представляют также нитраты - производные азотной кислоты (азотнокислый натрий - NaNO3), вещества, содержащие в молекуле нитрогруппу. Попав в организм эти вещества могут превращаться в нитриты. В печени это превращение активирует глутатион-зависимая нитратредуктаза; в желудочно-кишечном тракте ряд микроорганизмов, таких как Escherichia coli, Pseudomonas aurogenosa и др. обладают способностью восстанавливать нитраты до нитритов.
Основные источники нитратов в пище - овощи, мясные продукты, фрукты, соки. Большое количество нитратов в сельской местности может содержаться в колодезной воде. Причина этого - проникновение в воду поверхностных вод, кантаминированных нитрат-содержащими удобрениями. Ретроспективные исследования показали, что уровень нитратов в питьевой воде не должен превышать 45 ppm (в пересчёте на NO3).
Особенно чувствительны к нитратам дети. Впервые метгемоглобинемия у грудных детей, вызванная питьевой водой, содержащей нитраты, описана в 1945г. Comly. Причины явления обусловлены низкой кислотностью желудка и, как следствие этого, высокой активностью нитрат-редуцирующей флоры кишечника, пониженной (вплоть до 4 месячного возраста) активностью НАДН-метгемоглобинредуктазы, более высоким, в сравнении со взрослыми, потреблением жидкости на килограмм массы. Наконец, детям, как правило, дают воду после кипячения, вследствие чего концентрация нитратов в ней повышается.
2.1.3. Проявления метгемоглобинемии
Выраженность симптомов зависит от содержания метгемоглобина в крови. Основным проявлением является цианоз кожных покровов и видимых слизистых. Цвет цианотичных участков кожи от синеватого до шоколадного; слизистые более коричневого, чем синего цвета.
Необходимо отличать периферический и центральный цианоз.
Периферический цианоз является следствием нарушения гемодинамики и недостаточной гемоперфузии периферических органов. Наиболее ранние проявления - синюшная окраска носа и ногтевых лож. Причина цианоза - избыточное содержание восстановленного гемоглобина вследствие усиленной экстракции кислорода тканями, плохо снабжаемыми кровью (сердечная недостаточность).
Центральный цианоз развивается при повышенном содержании в крови сульфогемоглобина (более 0,5г на децилитр), метгемоглобина (более 1,5г на децилитр) и восстановленного гемоглобина (более 5г на децилитр). При содержании метгемоглобина менее 15% цианоз отсутствует. Проявления гипоксии формируются при метгемоглобинемии более 55%. Симптомы, развивающиеся на фоне метгемоглобинобразования представлены на таблице 3.
Таблица 3. Проявления метгемоглобинемии различной степени выраженности
Содержание метгемоглобина (%) |
Проявления |
0 - 15 |
Отсутствуют |
15 - 20 |
"шоколадная кровь", цианоз |
20 - 45 |
Возбужденность, одышка при физической нагрузке, слабость, утомляемость, беспокойство, оглушенность, головная боль, тахикардия |
45 - 55 |
Угнетение сознания |
55 - 70 |
Ступор, судороги, кома, брадикардия, аритмии |
> 70 |
Сердечная недостаточность, смерть |
При периферическом цианозе и повышенном содержании восстановленного гемоглобина в крови показана ингаляция кислорода. При наличии метгемоглобина или сульфогемоглобина в крови оксигенотерапия не приводит к устранения цианоза.
Отдельные ксенобиотики способны, в зависимости от условий вызывать образование как сульф-, так и метгемоглобина. Образование сульфгемоглобина сдвигает кривую диссоциации оксигемоглбина вправо, т. е. происходит облегчение отдачи кислорода кровью тканям. В этой связи на фоне выраженного цианоза отмечается лишь незначительная одышка. Артериальная кровь приобретает коричневатый оттенок. Как правило сульфгемоглобинемия не достигает уровня опасного для жизни. Дифференцировать сульфгемоглобинемию от метгемоглобинемии можно с помощью спектрофотометрических методов исследования крови.
2.1.4. Лабораторная диагностика
Ряд простейших методических приёмов позволяет иногда выявить наличие метгемоглобина в крови. Если пигмента в крови более 15%, капля крови окрашивает фильтровальную бумажку в "шоколадный" цвет, хорошо выявляемый при сравнении с цветом нормальной крови. Пропускание кислорода через венозную кровь изменяет её вишневый цвет на алый. Кровь, содержащая метгемоглобин, не меняет при этом окраску. Наконец, добавление к разведённой в 100 раз крови, содержащей метгемоглобин, кристалика цианистого калия приводит её к окрашиванию в розовый цвет в следствие образования цианметгемоглобина. Диагностическими признаками массивного метгемоглобинообразования является коричнево-черное окрашивание мочи, а также появления в ней белка.
Результаты анализа газового состава крови следует оценивать с большой осторожностью. Часто данные о сатурации крови кислородом получаются на основе измерения парциального давления газа в плазме крови. Необходимо помнить, что присутствие метгемоглобина или сульфгемоглобина не сказывается на этом показателе. Некоторые оксиметры позволяют измерить фракционную сатурацию. В этих случаях оценивают отношение количества оксигемоглобина к общему количеству гемоглобина (оксигемоглобин, восстановленный гемоглобин, метгемоглобин, карбоксигемоглобин). Однако большинство оксиметров позволяют оценить только функциональную сатурацию гемоглобина, т.е. соотношение гемоглобина и восстановленного гемоглобина. Такие приборы дают информацию о достаточном содержании кислорода в крови даже при очень высокой степени метгемоглобинемии.
С помощью спектрофотометрических исследований можно отличить (как указывалось) метгемоглобин от сульфгемоглобина, а также определить процентное содержание метгемоглобина в крови. Если время прошедшее от момента забора крови и исследованием продолжительное, результат может оказаться ложным, так как процессы окисления и восстановления гемоглобина проходят и in vitro. Необходимо помнить, что у больных с выраженной анемией даже незначительное содержание метгемоглобина в крови может вызвать глубокую гипоксию. Поэтому обследование должно обязательно сопровождаться подсчетом эритроцитов и определением общего гемоглобина.
2.1.5. Принципы оказания помощи
Лечение острых интоксикаций метгемоглобинообразователями включает предотвращение дальнейшего поступления ксенобиотика в организм, оксигенацию крови, введение средств, превращающих метгемоглобин в гемоглобин, нормализацию кислотно-основного равновесия, поддерживающую, симптоматическую терапию. При авариях на производствах, сопровождающихся проливами токсикантов, необходимо проводить полную санитарную обработку пораженных. Лечение показано при появлении признаков интоксикации (таблица 2).
Антидотом метгемоглобинообразователей является метиленовый синий (тетраметилтионин хлорид). Препарат назначают лицам с уровнем метгемоглобинемии более 30%. В случае сопутствующей анемии, показатель может быть значительно ниже. Метиленовый синий играет роль дополнительного кофактора, передающего электрон от НАДФН на метгемоглобин, восстанавливая последний в течение 1 - 2 часов. В процессе реакции образуется его лейкоформа. Следовательно, для того, чтобы препарат выполнял функции антидота, необходимо нормальное содержание НАДФН в эритроцитах (рисунок 5). Окислительно-восстанолвительная система, формируемая метиленовым синим и его лейкоформой действует обратимо и при избытке окисленной формы (введение необоснованно высокой дозы препарата) может произойти дополнительное метгемоглобинообразование. При назначении препарата лицам с дефицитом Г-6Ф-ДГ и низким содержанием НАДФН в эритроцитах, возможен гемолиз.

Рисунок 5. Восстановление метгемоглобина при участии метиленового синего и метгемоглобинредуктазы
Метиленовый синий вводят внутривенно в количестве 0.1 - 0.2 мл/кг 1% раствора (1 - 2 мг/кг). Если симптомы интоксикации не устраняются, через час следует повторить введение. Рекомендуется перед повторным введением определить уровень метгемоглобина в крови. Наиболее частой причиной резистентности патологии к препарату является дефицит Г-6Ф-ДГ, НАДФН-метгемоглобинредуктазы, а также сулфметгемоглобинемия. У леченых больных в течение некоторого времени после исчезновения симптоматики может сохраняться цианоз, что обусловлено с одной стороны способностью препарата окрашивать кожу, с другой бессимптомным течением метгемоглобинемии с уровнем менее 30%. Токсичными дозами метиленовой сини являются 7 - 15 мг/кг. Как уже указывалось, причина токсического действия состоит в способности окисленной формы вещества окислять гемоглобин. Развиваются гемолиз, гипербилирубинемия, ретикулоцитоз, анемия, иногда в крови появляются тельца Гейнца. Побочные эффекты, развивающиеся при использовании метиленового синего включают беспокойство, головную боль, спутанность сознания, тошноту, рвоту, абдоминальные боли, тремор, учащение сердцебиений. На ЭКГ - снижение амплитуды зубцов Т и R.
Непосредственно взаимодействовать с токсикантами в эритроцитах способна аскорбиновая кислота. Однако скорость процесса низка, и в этой связи препарат назначают лишь в случае метгемоглобинемии, обусловленной дефицитом редуктаз.
2.2. Образование карбоксигемоглобина
Карбоксигемоглобин образуется при действии на организм монооксида углерода (СО), так называемого угарного газа, а также при отравлении карбонилами металлов, прежде всего никеля и железа (Ni(CO)4; Fe(CO)5).
СО представляет собой бесцветный газ, лишенный запаха. Основным источником его являются процессы неполного сгорания топлива (древесины, угля, газа, бензина, дизельного топлива и т.д.), поэтому вещество содержится в больших количествах в выхлопных газах двигателей автомобилей, в атмосфере плохо вентилируемых производственных и бытовых помещений, в которых эксплуатируют устройства по сжиганию топлива, в воздухе помещений, охваченных пожаром. Единственный способ поступления газа в организм - ингаляционный.
Сродство монооксида углерода к гемоглобину в 200 - 300 раз выше, чем у кислорода, поэтому при поступлении в организм вещество связывается с двухвалентным железом гемоглобина, с образованием карбоксигемоглобина, не способного к транспорту кислорода. Развивается гипоксия:
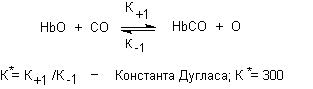
Появление карбоксигемоглобина в крови нарушает явление гем-гем взаимодействия (константа Хила становится равной 1,0), что затрудняет диссоциацию оксигемоглобина и в еще большей степени ухудшает оксигенацию тканей. Тяжесть клинической картины отравления угарным газом определяется:
-содержанием карбоксигемоглобина в крови;
-потребностью организма в кислороде;
-интенсивностью физической активности пострадавшего.
В состоянии равновесия СО, в концентрации 1 объемная часть на 1500 объемных частей воздуха, превращает 50% гемоглобина крови экспериментальных животных в карбоксигемоглобин. Как правило в реальных условиях, концентрация 0,1% СО во вдыхаемом воздухе обусловливает образование около 10% карбоксигемоглобина в крови. Экспозиция 0,5% СО в течение часа при умеренной физической активности сопровождается образованием 20% карбоксигемоглобина, при этом пострадавший начинает испытывать неприятные ощущения, предъявляет жалобы на головную боль. Интоксикация средней степени тяжести развивается при содержании крабоксигемоглобина 30 - 50%, тжелая - около 60%, смертельная - более 66%.
Связь СО с гемоглобином обратима. Поэтому при удалении пострадавшего из атмосферы, содержащей газ, происходит его быстрая элиминация из организма.
Имеются данные, что СО взаимодействует также с миоглобином тканей (сродство в 14 - 50 раз выше, чем к кислороду), пероксидазой, медь-содержащими ферментами (тирозиназа), различными цитохромами (в том числе цитохромом а, цитохромом Р-450 и т.д.).
Основные клинические проявления развиваются со стороны ЦНС. Признаками интоксикации являются тошнота, рвота, головная боль, беспокойство, спутанность сознания, а в тяжелых случаях - кома. Вследствие гипоксии развивается отек мозга, гипертензия, сменяющаяся гипотонией. Нередко отмечаются деструктивные процессы в ткани мозга, приводящие к формированию стойких нарушений функций ЦНС.
К числу других, наиболее часто встречающихся проявлений острого поражения СО относятся: изменение окраски кожных покровов (розовая), тахикардия, аритмии, ишемия и инфаркт миокарда; умеренный отек легких, буллезные высыпания на коже, рабдомиолиз с последующей острой почечной недостаточностью.
Основой оказания помощи отравленному в ранние сроки является ингаляция кислорода под повышенным давлением, что позволяет вытеснить СО из связи с гемоглобином. Критерием для проведения гипербарооксигенации является содержание в крови более 25% карбоксигемоглобина.
3. Изменение числа форменных элементов
Токсическое действие некоторых веществ может сопровождаться существенным нарушением клеточного состава крови. Наиболее значимыми проявлениями интоксикаций являются: анемии (гемолитическая, апластическая), лейкопении, тромбоцитопении, лейкемии.
3.1. Гемолитические анемии
Среди анемий химической этиологии, гемолитические - встречаются наиболее часто. Вещества, вызывающие внутрисосудистый гемолиз можно разделить на три группы (таблица 4):
1. Разрушающие эритроциты (при определённой дозе) у всех отравленных;
2. Гемолизирующие форменные элементы у лиц с врождённой недостаточностью Г-6Ф-ДГ;
3. Вызывающие иммунные гемолитические анемии.
Таблица 4. Вещества, вызывающие гемолиз
1. Общие гемолитики
анилин сурма арсин (мышьяковистый водород) бромат калия бензол хлорат калия (натрия) хлористый метил хлороформ медь динитробензол фенол гидрохинон лецитин мезантоин |
нафтален нитриты нитраты свинец сульфоны толуол трибромметанол тринитробензол тринитротолуол нитробензол цинкэтиленбисдитиокарбамат Яды пауков Яды змей (кобра) |
2. Токсиканты, вызывающие гемолиз у лиц с дефицитом Г-6Ф-ДГ
ацетанилид ацетилсалициловая кислота аскорбиновая кислота гидразин метиленовый синий хлорамфеникол дифенилсульфон фенилгидразин фуразолидин |
Н-ацетилсульфамид нафтален нитрофурантион примахин сульфаметоксипиридазин сульфаниламиды сульфапиридин тиозосульфон |
3. Токсиканты, вызывающие иммуноаллергические гемолитические анемии
парааминосалициловая кислота альфаметилдофа цефалоспорины хинидин хинин хлордиазепоксид хлорпромазин хлорпропамид дифенилгидантион фенацетин |
фенилбутазон индометацин изониазид меолфалан пенициллин рифампицин стибофен сульфониламиды толбутамид |
Часть веществ, относящихся к первой группе, такие как бензол, толуол, динитробензол, хлороформ действуют непосредственно на мембрану эритроцитов разрушая её. Другие являются метгемоглобинообразователями, и развивающийся при интоксикации ими гемолиз является вторичным явлением. Особенно чувствительны к таким токсикантам лица с дефицитом глутатионредуктазы и Г-6-ФД (см. выше), что объединяет их с веществами составляющими вторую группу. Действуя в высоких дозах, препараты второй группы вызывают гемолиз и у лиц без дефектов энзимов. Таким образом различие между группами достаточно условно.
В основе иммунологических анемий лежат два механизма. Первый связан с фиксацией токсиканта на мембране эритроцита с образованием комплексного антигена. Гемолиз развивается вследствие атаки изменённых мембран эритроцитов антителами (IgG) в присутствии комплемента. Второй механизм состоит в образовании комплексного антигена токсикант-белок плазмы крови. После фиксации комплексного антигена на мембране эритроцитов также в присутствии антител (IgM) и комплемента происходит их гемолиз. Во втором случае гемолиз происходит более бурно, но, как правило, иммуноаллергические анемии, в целом, выражены умеренно. Примером токсикантов, действующих по первому механизму является пенициллин, по второму - хинин, хинидин.
Гемолитики разрушают эритроциты и гемоглобин выходит в плазму крови. Растворенный в плазме гемоглобин способен связывать кислород в такой же степени, как и заключенный в эритроциты. Поэтому в первые часы после острого воздействия токсикантов клиника гипоксии практически не выражена. Однако гемолиз сопровождается:
- существенным повышением коллоидно-осмотических свойств крови (содержание белка в плазме возрастает с 7 до 20%);
- ускоренным разрушением гемоглобина. В эритроцитах гемоглобин сохраняется в среднем около 100 дней, т.е. весь период жизни клетки. В случае тяжелого гемолиза, когда содержание эритроцитов падает до 800 тыс. в мм3, уже через сутки уровень Нb составляет менее 30% от нормы;
- затруднением диссоциации оксигемоглобина и, следовательно, ухудшением оксигенации тканей. Одна из причин явления существенно более низкое содержание в плазме крови, в сравнении с эритроцитами, основного биорегулятора сродства кислорода к гемоглобину - 2,3-дифосфоглицерата;
- нефротоксическим действие гемоглобина, свободно циркулирующего в плазме крови.
Указанные особенности являются важными элементами патогенеза острых интоксикаций гемолитиками.
3.1.2. Краткая характеристика некоторых токсикантов
3.1.2.1. Мышьяковистый водород (Арсин - AsH3)
Арсин - бесцветный газ, без запаха. Используется в химическом синтезе, а также выделяется при зарядке аккумуляторных батарей. Острое воздействие арсином в высоких концентрациях сопровождается быстрым развитием гемолиза с последующим формированием почечной недостаточности. В ходе различных аварий на производствах отравление получили несколько сот человек. Летальность составляет более 20%. Экспериментально установлено, что гемолитический эффект обусловлен снижением содержания глутатиона в эритроцитах. Кратковременная ингаляция токсиканта в концентрации 250ppm, а также ингаляция в течение 30 мин арсина в концентрации 25 - 50ppm смертельна; 10ppm вызывает гибель пострадавших при длительной многодневной ингаляции. Кривая токсичности арсина характеризуется большой крутизной, это означает, что различия доз, вызывающих пороговое действие и смертельное поражение, малы. Так, в опытах на животных показано, что ингаляционное воздействие токсикантом в течение 28 дней в концентрации 5ppm переносится практически бессимптомно. Вместе с тем ингаляция в течение 4 суток вещества в концентрации 10ppm приводит к 100% гибели животных. Такая закономерность соответствует представлениям о механизме токсического действия вещества. Глутатион, как известно, необходим для поддержания целостности мембраны эритроцитов. Если скорость его синтеза превышает скорость истощения, наступающего под влиянием арсина, гемолиз не развивается. Напротив, если истощение превалирует над синтезом, развивается острая гемолитическая реакция. Наконец, в тех случаях, когда воздействие AsH3 не сопровождается полным истощением запасов восстановленного глутатиона, гемолитический эффект носит дозо-зависимый характер.
В опытах на мышах показано, что воздействие арсином в течение 1 часа в концентрации от 5 ppm до 26 ppm сопровождается эффектами от пороговых до смертельного. Отмечается, что максимальное снижение содержания эритроцитов в крови у выживших животных наступает через сутки после воздействия, а восстановление их числа до нормы - к 11 суткам. Во всех случаях воздействия арсином, сопровождавшихся гемолизом, отмечали существенное истощение содержания глутатиона в эритроцитах.
Снижение осмотической стойкости эритроцитов отмечается лишь при действии арсина в высоких концентрациях (15ppm - 25ppm). Этот эффект может быть использован в качестве биотеста на действие токсиканта.
Периоду клинических проявлений интоксикации предшествует скрытый период. Как правило более короткому скрытому периоду соответствует более тяжелое течение интоксикации.
У животных, отравленных арсином, отмечается существенное увеличение активности кислой дегидрогеназы
Клинические признаки и проявления отравления арсином отражают процессы, связанные с развивающимся гемолизом эритроцитов. Арсин не вызывает явлений раздражения слизистых оболочек в концентрации до 2 ppm. В этой связи контакт с веществом в относительно высоких концентрации может проходить практически бессимптомно. Первые признаки интоксикации включают гемоглобинурию, беспокойство, слабость, тошноту, рвоту, схваткообразные боли в животе. После скрытого периода, обычно продолжающегося от 2 до 24 часов, появляется желтуха, сопровождающаяся анурией или олигурией. Отмечается угнетение эритроидного ростка костного мозга. Особенно чувствительны к действию арсина лица с дефицитом Г-6Ф-ДГ, сердечной и почечной недостаточностью. Характерна триада симптомов: анемия, боли в животе, гематурия. Частым осложнением отравления является токсический отёк лёгких.
Лечение начинается немедленно после удаления пострадавшего из зараженной атмосферы. При содержании гемоглобина в плазме крови более 1,5 мг/ мл показано обменное переливание крови. В плане профилактики почечной недостаточности, в случае развития гемолиза, эффективным может оказаться мероприятие по ощелачиванию мочи. Использование хелатирующих агентов при отравлении арсином оказывается малоэффективным.
При хронической интоксикации возможно развитие сердечной недостаточности, постинтоксикационной нейропатии, легких психоорганических изменений. Однако чаще подобные явления сопутствуют острой интоксикации. В отдельных случаях нейропатия развивается спустя 1 - 6 месяцев после острого воздействия арсином.
Средневзвешенное во времени значение предельного порога воздействия арсина (TLY - TWA: Threshold Limit Value - Time-Weighted Average) для рабочего мест в США составляет 0,05 ppm. Это пороговое значение определяется как концентрация токсиканта, при которой все рабочие могут подвергаться действию вещества в течение всего периода работы (до выхода на пенсию) с учетом 8-часового рабочего дня, и при этом неблагоприятные эффекты развиваться не должны.
3.1.2.2. Сурмянистый водород (Стибин - SbH3)
Стибин образуется при действии водорода на сурьму. Это бесцветный газ без вкуса и запаха. Действуя ингаляционно, вещество вызывает гемолиз, сопровождающийся вторичным поражением печени и почек. Проявления интоксикации: гематурия, тошнота, рвота, желтуха, шок, признаки острой почечной недостаточности. Лечение симптоматическое. Как и при интоксикации арсином, в случае массивного гемолиза, показано обменное переливание крови.
3.1.2.3. Тринитротолуол
Отравления тринитротолуолом встречаются на производствах взрывчатых веществ и при воздействии пороховых газов. Основные пути поступления в организм: ингаляционный и через кожу. Проявления гематотоксического действия вещества: анемия смешанного типа (апластическая с элементами гемолитической), метгемоглобинообразование. Одновременно отмечаются дерматит, гастрит, токсический гепатит.
3.1.3. Биомониторинг
Система биомониторинга воздействия арсина, стибина и других промышленных гемолитиков разработаны недостаточно, поскольку отсутствуют специфические проявления действия этих веществ в минимальных дозах. Для выявления действия арсина полезным может оказаться определение суммарного мышьяка в моче. В норме содержание элемента не должно превышать 50 мкг/ л.
Для выявления действия стибина можно использовать выявление сурьмы в крови и моче. Нормальным содержанием элемента в цельной крови является 3 мкг/ л, в плазме крови 0,3 мкг/ л, в суточной моче - 0,5 - 2,6 мкг/ л.
3.2. Аплазия костного мозга
Острые и хронические отравления могут приводить к развитию апластических процессов в костном мозге. При этом, как правило, снижается содержание и эритроцитов, и лейкоцитов, и тромбоцитов, развивается панцитопенический синдром. Некоторые токсиканты, например бензол, могут провоцировать гемопоэтические расстройства не только апластического, но и гиперпластического типа. При интоксикации такими веществами последствия определяются дозой, условиями действия, индивидуальной чувствительностью к токсиканту, продолжительностью жизни зрелых форменных элементов крови и проявляются панцитопенией, лимфопенией, апластической анемией, миелоидной метаплазией, лейкемоидной реакцией и настоящей лейкемией. Изолированное подавление числа форменных элементов одного типа встречается при интоксикациях чрезвычайно редко. Как правило об апластической анемии, токсическом агранулоцитозе, токсической тромбоцитопении говорят в тех случаях, когда сокращение данного типа клеток является основным гематологическим признаком отравления.
Сокращение числа форменных элементов крови может быть результатом действия огромного числа токсикантов, как лекарственных веществ, так и промышленных ядов и веществ природного происхождения.
В зависимости от воспроизводимости наблюдаемого эффекта вещества делятся на две группы. Ограниченное их число вызывает апластический процесс во всех случаях действия в определённой дозе. Вторая группа химических веществ, по большей части это медикаменты, вызывает аплазию костного мозга лишь у ограниченной части людей и нередко только после повторного приёма. Так, риск фатальной апластической анемии у лиц, леченных хлорамфениколом, составляет 1 : 20000 - 30000; фенотиазины вызывают агранулоцитоз с частотой 1 : 1200. Некоторые вещества, относящиеся к первой группе, представлены на таблице 5.
Таблица 5. Химические агенты, нарушающие клеточный состав крови
А. Алкилирующие агенты: -сернистый иприт -кислородный иприт -азотистый иприт и его производные(циклофрсфамид и др.) -дериваты этиленимина (триметамин, инпрокон) -эфиры метансульфоновой кислоты (цитосульфан, цитостоп) -метилгидразин и его производные(ибентизин) -производные алкилмочевины (ломустин) -этиленоксид Б. Антиметаболиты: -производные пиперидина (аминоптерин) -производные пурина (азатиоприн) -производные пиримидина (фторафур) |
В. Другие цитостатики: -цитостатики растительного происхождения (колхицин, винглицин, винкристин) -антибиотики цитостатического действия (актиномицин, оливомицин, пуромицин) Г.Промышленные агенты и экотокстиканты: -свинец -мышьяк -эфиры гликоля -тринитротолуол -органические растворители -1,3-бутадиен -хлордан, гептахлор -2,4-Д; 2,4,5-Т -бензол |
В основе токсического действия препаратов первой группы лежит их способность подавлять обмен ДНК и РНК (сернистый, кислородный, азотистый иприты и др.), нарушать процесс митотического деления клеток (винкристин, винбластин и др.), блокировать синтез белка (пуромицин и др.) в клетках эритроидного (анемия), миелоидного (агранулоцитоз) и мегакарицитарного (тромбоцитопения) ростков. Механизмы действия веществ второй группы по большей части обусловлены иммуноаллергическими процессами, либо связаны с врожденными пороками метаболизма ксенобиотиков, другими особенностями токсикокинетики.
3.2.1. Основные проявления интоксикаций
3.2.1.1. Панцитопения.
Основные признаки панцитопении: состояние слабости и усталости, развивающихся в следствие анемии; лихорадка, инфекционные осложнения, как результат нейтропении; кровотечения - последствия тромбоцитопении. При обследовании отмечается бледность кожных покровов, кровоточивость десен, пурпура. В тяжелых случаях - воспалительные процессы в ротовой полости. Костный мозг беден клеточными элементами. На миелограмме доминируют лимфоциты и ретикулярные клетки. Отмечается жировое перерождение костного мозга, фиброз. В крови - снижение количества эритроцитов (менее 2000000 в мм3); гранулоцитопения - количество лейкоцитов снижается до 1500 и менее клеток в мм3 крови; относительный лимфоцитоз; тромбоцитопения.
3.2.1.2. Агранулоцитоз
При типичном агранулоцитозе доминирующим признаком является гранулоцитопения. В тяжелых случаях количество лейкоцитов снижается до 500 - 300 клеток в мм3 крови. Отмечается относительный лимфоцитоз. Количество гранулоцитов может составлять менее 2% от общего числа лейкоцитов. При исследовании пунктатов костного мозга выявляется существенное снижение клеток миелоидного ряда, особенно нейтрофильных метамиелоцитов и миелоцитов. Клинически патология проявляется прежде всего инфекционными осложнениями: некротическими поражениями слизистой ротовой полости (десны, миндалины, мягкое нёбо, глотка), некротической ангиной. Прогрессирование заболевания манифестируется утяжелением инфекционных осложнений, вплоть до развития сепсиса. Течение патологического процесса в значительной степени определяется особенностями токсического действия вещества, вызвавшего гранулоцитопению.
3.2.1.3. Тромбоцитопения
Тромбоцитопения, связанная с действием токсикантов, проявляется кровотечениями различной степени тяжести. Признаки геморрагии: петехии, пурпура, геморрагические пузыри на слизистой полости рта, желудочно-кишечные кровотечения. При аллергических процессах количество тромбоцитов в тяжелых случаях падает до 1000 и менее в мм3 крови, при этом число мегакариоцитов в костном мозге снижается несущественно. Геморрагическому синдрому сопутствует анемизация организма.
3.3. Лейкемии
3.3.1. Распространённость
В США ежегодно регистрируется около 24000 новых случаев лейкемий, что составляет примерно 3% от общего количества новообразований. Острая миелоидная лейкемия (ОМЛ) и её разновидности составляют 46% всех лейкемий; хроническая миелоидная лейкемия (ХМЛ) - 14%; острая лимфоидная лейкемия (ОЛЛ) - 13%; хроническая лимфоидная лейкемия (ХЛЛ) - 29%. Приведенные цифры близки для большинства развитых в промышленном отношении стран. У взрослых ОМЛ составляет примерно 90% всех лейкемий. Все известные этиологические факторы, провоцирующие развитие лейкемий, включая химический, являются причиной лишь незначительной части формирующихся случаев заболеваний.
Вторичная острая миелоидная лейкемия - достаточно хорошо установленный феномен. Она является основным злокачественным заболеванием крови, формирующимся на фоне лечения новообразований цитостатиками из группы алкилирующих агентов. Частота развития вторичной ОМЛ, в зависимости от дозы, назначаемого дополнительно, лучевого облучения, колеблется в интервале от 0,3 до 20%.
Попытки установить причинно-следственные связи между фактом действия токсиканта и возникновением лейкемий связаны с большими трудностями. Одна из них обусловлена пересмотром классификации патологических состояний. С одной стороны, патологи стремятся дать всё более детальную характеристику, основываясь на индивидуальных клеточных типах, нерегулируемая пролиферация которых лежит в основе лейкемий. С другой стороны, в ходе эпидемиологических исследований просматривается стремление группировать сравнительно редко встречающиеся типы неоплазмы, с тем, чтобы иметь репрезентативные группы для проведения анализа. Такая дивергенция интересов невольно приводит к ошибкам, особенно в тех случаях, когда этиология и патогенез новообразований, объединенных искусственно в единую группу, на самом деле различны. Не смотря на определённый прогресс в этой области, большинство популяционных исследований опирается на архаичные классификации лейкемий, что существенно снижает научную значимость формулируемых выводов.
3.3.2. Диагноз
Достижения клеточной и молекулярной биологии привело к существенному увеличению числа классификационных подтипов миелоидных и лимфоидных лейкемий, основывающихся на фено- и генотипическом анализе. В этой связи сравнение результатов старых и современных исследований, направленных на установление причинно-следственных связей в системе токсикант - неоплазма, порой весьма затруднены. В настоящее время следует констатировать, что проведение подобных исследований без детализации диагноза заболевания крови лишено смысла.
При проведении исследований необходимо иметь в виду существенные различия в частоте миелодисплазий у представителей различных возрастных групп. Так, у лиц в возрасте 20 - 29 лет она составляет 0,061 на 100000, у лиц в возрасте 70 - 79 лет - 19,58 на 100000.
3.3.3. Профессиональные воздействия и лейкемии
Целый ряд веществ рассматривается как потенциальные агенты, вызывающие лейкемии. В ряде случаев причинно-следственная связь между определённой профессиональной деятельностью и увеличением риска развития лейкемий установлена с большой степенью надёжности, однако природа веществ, которые обусловливают эту связь, остаётся не выясненной. Так, в ходе многочисленных эпидемиологических исследований установлен факт повышения частоты формирования лейкемий у работников предприятий по производству резины и резиновых изделий. В большинстве таких исследований это связывают с действием бензола. Однако, помимо этого токсиканта на производстве на человека могут действовать и иные факторы, а доказательства того, что именно бензол ответственен за увеличение риска развития заболеваний, строго говоря отсутствуют. По данным ряда авторов причинами лейкемий могу быть даже такие распространенные органические растворители, как четырёххлористый углерод, сероуглерод.
Увеличение числа лейкемий, преимущественно ОМЛ, отмечается среди рабочих металлургической промышленности, других сфер деятельности, при которых возможна ингаляция паров и аэрозолей металлов, однако не исключена возможность и иных, не выясненных до настоящего времени, этиологических факторов.
3.4. Характеристика наиболее известных токсикантов, вызывающих патологию крови
До настоящего времени бензол остаётся основным этиологическим фактором, вызывающим патологию крови. Однако в последнее время большое внимание уделяется и другим токсикантам, среди которых: свинец, мышьяк, радий, этиленоксид, некоторые пестициды (хлордан, гептахлор, 2,4-Д; 2,4,5-Т) этиленгликоль, 1,3-бутадиен.
3.4.1. Бензол
Помимо химического синтеза, бензол широко используется в качестве растворителя особенно в производстве клеев, в кожевенной промышленности, при производстве резины и резиновых изделий, в нефтеперерабатывающей промышленности, производстве химикалиев, пестицидов и пластмасс. Интоксикация веществом возможна, кроме того, на складах горюче-смазочных материалов, в фармацевтической промышленности. После установления токсического действия бензола на костный мозг его по возможности стали заменять на менее токсичные ксилол и толуол. Установление гигиенических нормативов и контроля за их соблюдением существенно сократили последствия токсического действия вещества, тем не менее полностью устранить неблагоприятное действие токсиканта на здоровье людей при контакте с бензолом пока не удаётся. Особенно велик риск поражения при транспортировке бензола, замене и чистке химических реакторов, клапанов, трубопроводов и т.д.
Основной путь поступления бензола в организм человека на производстве - ингаляционный. Кожа обычно не является значимыми входными воротами для токсиканта, хотя длительное воздействие на кожу чистого вещества и его аэрозоля могут привести к интоксикации.
Поступившее во внутренние среды организма вещество быстро выводится из организма практически в неизменённом виде через лёгкие и в форме конъюгатов с мочой. Хотя молекула бензола проста, метаболизм его достаточно сложен. В настоящее время доказано, что угнетение костного мозга обусловлено действием метаболитов токсиканта. Начальные этапы метаболических превращений проходят в основном в печени при участии цитохром-Р450-зависимых оксидаз. Продуктом этих превращений является фенол. Превращение фенола под влиянием все тех же цитохром-Р450-зависимых оксидаз приводит к образованию полифенольных метаболитов, в основном гидрохинонов, а также, под влиянием пероксидаз, - бифенолов, гидрохинона, р-бензохинона. Долгое время полагали, что муконовый альдегид и муконовая кислота (НООССН=СНСН=СНСООН), в небольшом количестве выделяющиеся с мочой отравленных, играют ключевую роль в механизме токсического действия бензола. В настоящее время вопрос о механизме действия бензола полагают целесообразным считать открытым.
Ключевым ферментом, обеспечивающим токсическое действие бензола на костный мозг, вероятно следует считать миелопероксидазу, активность которой чрезвычайно высока в гранулоцитарных элементах костного мозга. Энзим катализирует превращение одного из метаболитов бензола - гидрохинона в высокоактивный 1,4-бензохинон. В процессе метаболизма активируются свободно-радикальные процессы в клетках.
В эксперименте показано, что одновременное с бензолом введение индометацина (антиоксидант и противовоспалительное средство) существенно ослабляет миелотоксическое действие вещества. Это указывает на значение простагландинсинтетазы (циклооксигеназы) для развития индуцируемого бензолом миелотоксического эффекта. Однако показано, что индометацин угнетает активность и миелопероксидазы (блокируется окисление гидрохинона).
Эффекты, связанные с хроническим действием бензола, практически полностью ограничиваются нарушениями со стороны гемопоэза и иммунной системы. Способность бензола угнетать кроветворение была обнаружена в начале 20 века. Это свойство вещества первоначально даже пытались использовать для лечения лейкемий, но безуспешно.
Признаками хронической интоксикации бензолом являются: анемия, тромбоцитопения, лимфоцитопения, панцитопения, сопровождающиеся слабостью, петехиальной сыпью, пурпурой, частыми инфекционными заболеваниями. Наиболее частое проявление - лейкопения, сопровождающаяся тромбоцитопенией. Часто, на фоне уменьшения числа форменных элементов в крови, выявляется гиперплазия костного мозга с признаками задержки созревания клеточных элементов эритроидного и миелоидного ряда. При обследовании рабочих типографий, контактировавших с бензолом в относительно высоких концентрациях, выявлены существенные нарушения со стороны системы крови (Greenberg, 1939; Goldwater et al, 1941). В крови обнаруживается относительная и абсолютная лимфопения, предшествующая анемии и тромбоцитопении. Гранулоциты, по-видимому оказываются более резистентными к действию токсиканта: гранулоцитопения, как самостоятельное проявление интоксикации, развивается редко.
По современным наблюдениям нарушения со стороны крови развиваются при хроническом действии бензола в концентрациях более 100ррм.
Бензол действует на клетки костного мозга, находящиеся в фазе G2 митоза. Эти представления находятся в соответствии с данными о высокой чувствительности цитоскелета (микротрубочки) к метаболитам бензола (гидрохинон, п-бензохинон), которые взаимодействуют с ГТФ-зависимыми структурами, вступая в ковалентную связь с сульфгидрильными группами белков. Эффекты метаболитов бензола не ограничиваются действием на клетки, находящиеся в фазе митоза. В сублетальных дозах возможно действие хинольных метаболитов на вхождение клеток в период клеточного деления.
Повторное введение бензола сопровождается уменьшением числа клеточных элементов в костном мозге. Эффект достигает максимума на 3 - 10 сутки и характеризуется исчезновением пула дифференцирующихся клеток средней степени зрелости. Характерной особенностью действия бензола является наличие рефрактерного периода, проявляющегося в том, что не смотря на продолжение его введения к 10 - 15 суткам отмечается нормализация клеточного состава костного мозга.
Путем введения метаболитов не удаётся воспроизвести клинику отравления бензолом. Так, введение даже больших доз фенола сопровождается лишь кратковременным угнетением кроветворения. Тем не менее, совместное введение фенола с гидрохиноном приводит к значимой супрессии клеточного деления в костном мозге. Вероятно, для воспроизведения полной картины интоксикации необходимо действие всего комплекса продуктов биотрансформации токсиканта.
3.4.2. Свинец
В прежние века свинец был доминирующей причиной хронических интоксикаций человека. Имеются данные, что конец Римской империи во многом связан с хронической интоксикацией населения свинцом, широко применявшимся для изготовления водопроводов и посуды. Изменившийся характер использования вещества в современном обществе, изменил и роль патологии, вызываемой токсикантом. В последние годы частота острых и хронических отравлений свинцом, сопровождающихся развитием выраженной патологии, существенно уменьшилась. И тем не менее полностью опасность поражения свинцом не исчезла. Особую проблему представляют красители на основе соединений свинца, свинецорганические соединения, такие как тетраэтил- и тетраметилсвинец, широко используемые в качестве добавок к горючим.
Одним из характерных проявлений хронической интоксикации свинцом является нарушения со стороны крови. Как в эксперименте, так и в клинике показано, что действие свинца на кровь ограничивается нарушениями со стороны эритроидного ростка. Характерный признак хронической интоксикации свинцом - анемия различной степени тяжести. В основе патологии лежат два основных механизма, это (1) угнетение эритропоэза в следствие нарушения процесса синтеза гема, опосредованное подавления активности дегидрогеназы
В условиях производства, связанного с воздействием свинца, у работающих порой отмечается незначительная анемия гипохромного характера с умеренным ретикулоцитозом. На ранних этапах развития интоксикации анемизации может предшествовать повышение содержания порфирина в клетках костного мозга и эритроцитах. Появление порфирина в моче, как правило, поздний признак интоксикации. В сомнительных случаях надёжными диагностическими признаками хронической интоксикации являются появление в моче
3.4.3. Мышьяк
Острые отравления мышьяком редко случаются в условиях производства. Основной путь поступления токсикантов, содержащих мышьяк, - с зараженной водой и пищей. Одним из признаков острой интоксикации, хотя и не основным, является нарушение созревания миелобластов, проявляющееся лейкопенией.
Скорость элиминации мышьяка из организма относительно высока. Период полувыведения составляет 1 - 3 суток. Основной путь выведения - через почки. В этой связи важным диагностическим признаком интоксикации в первые сутки является обнаружение элемента в плазме крови и моче.
Имеются сообщения, что хроническое действие мышьяка может приводить к развитию лейкемий, болезни Ходжкина.
3.4.4. Этиленоксид
Этиленоксид широко используют в качестве исходного продукта для целей химического синтеза, а также средства стерилизации различного оборудования. Интоксикации этиленоксидом случаются и в госпиталях при загрузке и разгрузке стерилизационных камер, в которых вещество используется в качестве стерилизующего агента. Этиленоксид действует на организм как окислитель и алкилирующий агент. При хроническом воздействии проявляются его свойства как мутагенна и цитотоксиканта. Эти эффекты зарегистрированы как у человека, так и у лабораторных животных. Лейкемогенное действие этиленоксида нельзя считать окончательно доказанным, хотя отдельные сообщения, указывающие на это свойство в литературе имеются.
3.4.5. Эфиры гликолей
Эфиры гликолей используют для производства растворителей, лаков, красок, чернил, антифризов. Обычно их рассматривают как малотоксичные вещества. Имеются сообщения о гематотоксичности эфиров гликолей у человека. Регистрируется тенденция к анемизации, гранулоцитопения. Иногда на фоне нормальных показателей периферической крови в костном мозге выявляются признаки миелоидной гипоплазии, повреждения стромы костного мозга, сидеробластоз. Эффекты выражены слабо и при соблюдении техники безопасности практически не проявляются.
3.4.6. Производные феноксиуксусной кислоты
Основными представителями этой группы веществ являются 2,4-дихлорфеноксиуксусная кислота и 2,4,5-трихлорфеноксиуксусная кислота. Эти широко используемые гербициды получили известность в годы войны США и Вьетнама, поскольку применялись американскими военными для уничтожения лесов и урожаев противника. В результате не только вьетнамцы, но и американские солдаты получили поражение этими веществами. Неблагоприятные последствия, в основном, связывали с ТХДД, содержавшимся в виде примеси в смеси гербицидов (оранжевая жидкость).
В последние годы проведено немало исследований направленных на установление неблагоприятного действия гербицидов. В некоторых работах показана способность веществ повышать риск заболевания лимфомой Ходжкина. Однако этот факт нельзя считать окончательно установленным.
4. Мониторинг состояния системы крови лиц, работающих в условиях опасных производств
Мониторинг состояния здоровья работающих на опасных производствах должен быть постоянным, а применяемые методы пригодны для осуществления массовых обследований. Многие гематологи полагают, что для этих целей вполне пригоден развернутый анализ крови. Напротив, профпатологи считают этот способ массового обследования работающих не достаточно информативным. В качестве аргументов выдвигаются следующие соображения. Во-первых количественный состав крови изменяется под влиянием большого числа факторов не химической природы. Во-вторых, далеко не всегда выявляется корреляция между степенью изменения количества форменных элементов в крови и дозой токсиканта. Однако, отсутствие нарушений со стороны крови при отравлениях, в частности бензолом, не означает отсутствия нарушений со стороны костного мозга. Вот почему продолжаются поиски простых, но более специфичных и информативных методов обследования людей, контактирующих с потенциально опасными веществами.
В качестве дополнительных методов обследования часто рекомендуют проводить:
- оценку количества хромосомных аберраций в клетка периферической крови (в случаях бессимптомного течения интоксикации бензолом, количество хромосомных аберраций существенно не увеличивается);
- изучение распределения эритроцитов по их размерам, чувствительный тест, позволяющий выявить макро- и микроцитоз (развивающиеся например в следствии химически обусловленного дефицита фолиевой кислоты, при хроническом алкоголизме и т.д.)
Во всех случаях нарушений со стороны периферической крови у лиц, контактирующих с гематотоксикантами необходимо проводить углубленное обследование.
<< Содержание |



 Федеральное государственное бюджетное учреждение науки
Федеральное государственное бюджетное учреждение науки